
升研教育考研频道为23考研、24考研的同学们整理了“西南科技大学2022年考研专业课真题:807物理化学I”的相关信息,希望对正在备考的你有所帮助。考研复习效率不高怎么办?自己备考抓不住重点?想报考985/211等热门院校,但是没把握?升研教育推出考研集训营,全日制封闭式面授,10余年授课经验的老师,浓厚的学习氛围助你冲击目标、一战上研!
西南科技大学2022年考研专业课真题:807物理化学I
适用专业:070300化学
一、单项选择题(每题2分,共40分)
1、已知氢气的临界温度和临界压力分别为Tc=33.3K,Pc=1.297x106Pa。有一氢气钢瓶,在298K时瓶内压力为98.0x106Pa,这时氢气的状态为( )。
A、液态
B、气态
C、气、液两相平衡
D、无法确定
2、一瓶盛有N2和H2的混合气体,当选择H2作为体系时,则环境为( )。
A、N2、瓶子及瓶外其他物质
B、瓶子及瓶外其他物质
C、N2和瓶子
D、N2
3、甲烷的燃烧热为一965.6kJ·mol-1,其相应的化学反应计量式为( )。
A.C(g)+4H(g)=CH4(g)
B.C(g)+2H2(g)=CH4(g)
C.CH4(g)+3/2O2(g)=CO(g)+2H2O(1)
D.CH4(g)+2O2(g)=CO2(g)+2H2O(1)
4、封闭体系的内能变化ΔU体系和环境的内能变化ΔU环境之间的关系为( )。
A、|ΔU体系|=|ΔU环境I
B、|ΔU体系|>|ΔU环境|
C、|ΔU体系|<|ΔU环境|
D、ΔU体系=ΔU环境
5、体系不做非体积功的等压过程,吸收的热Qp与体系焓变关系为( )。
A、Qp>ΔH
B、Qp<ΔH
C、Qp=ΔH
D、Qp=ΔU
6、1molO2(g)与2molH2(g)完全反应生成2molH2O(g),反应进度ξ为( )。
A、0.5mol
B、1mol
C、2mol
D、无法判断
7、根据熵增加原理,若从ΔS系统>0判断过程一定是自发过程,那么系统一定是( )。
A、封闭系统
B、敞开系统
C、隔离系统
D、非隔离系统
8、若要通过节流膨胀达到制冷效果,则要求μJ-T( )。
A、>0
B、=0
C、<0
D、无法确定
9、A和B两组分在等温等压下混合形成理想液态混合物时,则有( )。
A、OmixH=0
B、AmixA=0
C、AmixS=0
D、AmixG=0
10、下列偏微分中是偏摩尔量的是( )

11、A、B两液体混合物在T-χ图上出现最高点,则该混合物对Raoult定律产生( )。
A、正偏差
B、负偏差
C、没偏差
D、不确定
12、在温度T时,某化学反应的ArHΘm<0, ΔrSΘm>0,则其标准平衡常数KΘ(),且随温度的升高而( )。
A、大于1,不变
B、小于1,不变
C、大于1,变小
D、小于1,变大
13、根据某一反应的ΔrGΘm值,下列不能确定的是( )。
A、标准状态下自发变化的方向
B、在ΔrGΘm所对应的温度下的平衡位置
C、在标准状态下系统所能做的最大非膨胀功
D、提高温度对平衡的影响情况
14、当电流通过原电池或电解池时,电极电势将偏离平衡电极电势而发生极化。当电流密度增大时,通常将发生( )。
A、原电池的正极电势增高
B、原电池的负极电势增高
C、电解池的阳极电势减小
D、无法判断
15、有两个都是一级反应的平行反应: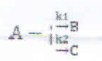 ,下列说法错误的是( )。
,下列说法错误的是( )。
A、k总=k1+k2
B、E总=E1+E2
C、k1/k2=[B]/[C]
D、t1/2=In2/(k1+k2)
16、对于一般的化学反应,当温度升高时,下面说法正确的是( )。
A、活化能明显降低
B、平衡常数一定变大
C、正、逆反应的速率系数成比例变化
D、反应到达平衡的时间变短
17、某化学反应的方程式为2A→P,则在动力学研究中表明该反应为( )。
A、二级反应
B、基元反应
C、双分子反应
D、以上都无法确定
18、把细长的两根木棍互相靠近(距离为d),平行地浮在水面上,用玻璃棒轻轻地在两木棍中间滴一滴肥皂液,两纸间的距离将( )。
A、增大
B、减小
C、不变
D、A.B.C都有可能
19、农药中加入一定量的表面活性物质,主要目的是( )。
A、增加农药的杀虫药性
B、提高农药对植物表面的润湿能力
C、防止农药挥发
D、消除药液的泡沫
20、气相中的大小相邻液泡相碰,两泡将发生的变化是( )。
A、大泡变大,小泡变小
B、大泡变小,小泡变大
C、大小泡均不变
D、两泡将分离开
二、填空题(每题3分,共45分)
1、范德华方程中的常数a是度量__的特征参数,常数b是度量__的特征参数。
2、T、p、V、U、H、S、G、W、Q等物理量中,_______属于状态函数。
3、运用盖斯定律计算过程热效应的前提是:(1)_____;(2)_______。
4、1mol单原子理想气体从p1,T1,V1等容冷却到p2,T2,V1,则该过程的ΔU___0,ΔS___0,W___0(填“>”,“=”或“<”)。
5、亨利定律的表示式是__。
6、蒸气压越大代表物质__挥发。(填“越难”或“越易”)
7、单组分系统中能平衡共存的最多相数是_____。
8、已知反应2NO(g)+O2(g)<->2NO2(g)是放热反应,当反应达到平衡时,要使平衡向右移动,应采用的手段是_______。
9、在强电解质的稀溶液中,摩尔电导率4m随浓度的增加而_____,电导率K随浓度的增加而____。(填“增大”或“减小”)
10、电解池是将___能转化为____能的装置。
11、强电解质MgCl2水溶液,其离子平均活度a±,与电解质活度aB之间的关系为____。
12、零级反应____基元反应。(填“是”或“不是”)
13、某反应进行完全所需时间是有限的,且等于C0/k(C0为反应物起始浓度),则该反应为___级反应。
14、已知某反应机理为: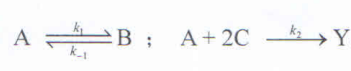 ,则Y的浓度随时间的变化率dCY/dt为_______。
,则Y的浓度随时间的变化率dCY/dt为_______。
三、计算题(共35分)
1、(本题12分)将1molN2(g,设为理想气体)从298K,100kPa的始态,经等温可逆压缩到600kPa,求该过程的Q,W,ΔU, ΔH,ΔS,ΔA,ΔG。
2、(本题8分)在400~500K,反应PCI5(g)=PCl3(g)+Cl2(g)的标准吉布斯自由能变化可由下式给出: ΔrGΘm/(J.mol-1)=83.68x103-14.52T/KxIn(T/K)-72.26T/K。试计算此反应在450K时的ΔrGΘm,ΔrHΘm,ΔrSΘm及KΘp。
3、(本题9分)设某电池的电池反应为Zn+CuSO4(aq)=Cu(s)+ZnSO4(aq)。在298K和313K时分别测得电池的电动势为1.1030V和1.0961V,并设在该温度范围内E随T的变化是均匀的。试求该电池在298K时反应的ΔrGΘm,ΔrHΘm,ΔrSΘm和可逆热效应QR。
4、(本题6分)药物阿司匹林的水解为一级反应。100°C下速率常数为7.92d-1,活化能为56.48kJ.mol-1。求:(1)100°C时水解反应的半衰期;(2)17℃时,阿斯匹林水解30%需多少时间?
四、简答题(5分)
为什么明矾能使浑浊的水很快变得澄清?
五、证明题(5分)
对于理想气体,试证明(δAm/δT)p=-(Sm+R)。
六、相图题(20分)
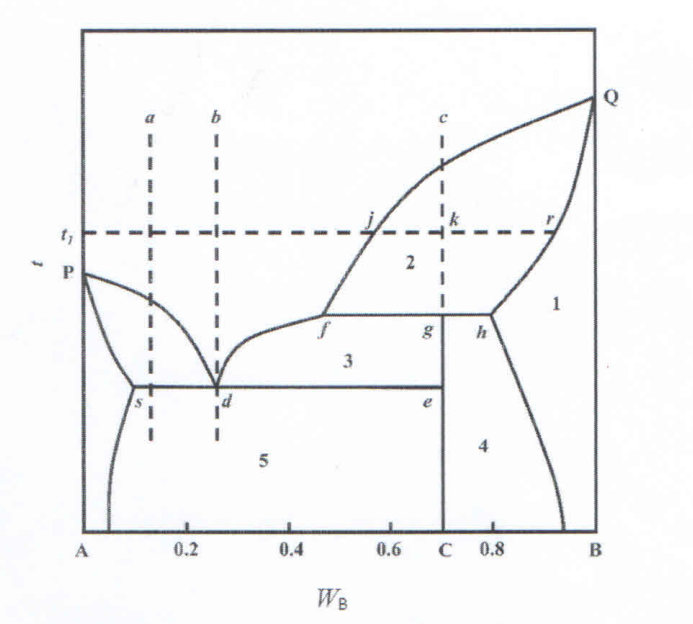
某A-B二组分凝聚系统在某压力下的相图如下图所示,其中C为不稳定化合物。
(1)标出图中1,2,3,4,5各相区的相态及组成和自由度数:
(2)指出图中的三相线及平衡关系;
(3)绘出图中状态点为a,b,c的样品的步冷曲线(无需注明冷却过程相变化);
(4)将5kg处于c点的样品冷却至t,系统中液态物质与析出固态物质的质量各为多少(已知j点对应的WB为0.6,c点对应的WB为0.7,r点对应的WB为0.9)?
【24考研辅导课程推荐】24考研集训营、周末辅导班、一对一辅导,相关课程都配有内部讲义及书籍资料,同时还有辅导老师进行学习规划及全程督学,详情可直接在线咨询。
免责声明:本站所提供的内容部分来源于网络搜集整理,由本站编辑上传,仅供个人研究、交流学习使用,不涉及商业盈利目的。如涉及版权问题,请联系本站管理员予以更改或删除。
距2024考研还剩天

三师服务丨全程规划丨大咖领学
三师服务丨全程规划丨大咖领学
三师服务丨全程规划丨大咖领学